1) การจัดเรียงอิเล็กตรอนเข้าระดับพลังงานหลัก
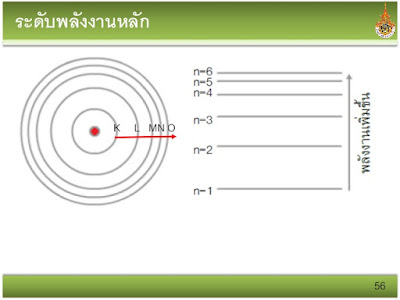
การจัดเรียงอิเล็กตรอนในระดับพลังงานหลัก
จำนวนอิเล็กตรอนในแต่ละระดับพลังงานหลักมีจำนวนไม่เกิน 2n2
เมื่อ n คือระดับพลังงานหลักที่ 1 , 2 , 3 , . . .
ระดับพลังงานหลัก n=1 มีอิเล็กตรอนไม่เกิน 2 อิเล็กตรอน
ระดับพลังงานหลัก n=2 มีอิเล็กตรอนไม่เกิน 8 อิเล็กตรอน
ระดับพลังงานหลัก n=3 มีอิเล็กตรอนไม่เกิน 18 อิเล็กตรอน
ระดับพลังงานหลัก n=4 มีอิเล็กตรอนไม่เกิน 32 อิเล็กตรอน
ตามความสัมพันธ์นี้การจัดเรียงอิเล็กตรอนในแต่ละระดับพลังงาน จะมีอิเล็กตรอนได้ไม่เกินจำนวนสูงสุดที่จะมีได้ ถ้าพิจารณา K และ Ca ซึ่งควรมีอิเล็กตรอนเป็น 2 , 8 , 9 และ 2 , 8 , 10 เนื่องจากในระดับพลังงานที่ 3 มีได้ถึง 18 อิเล็กตรอน แต่จากการศึกษาพบว่าการจัดเรียงอิเล็กตรอนของ K = 2 , 8 , 8 , 1 และ Ca = 2 , 8 , 8 , 2 เนื่องจากอิเล็กตรอนในระดับพลังงานที่ 3 ของทั้งสองธาตุมีเพียง 8 อิเล็กตรอน และส่วนที่เพิ่มขึ้นมาอีก 1 หรือ 2 อิเล็กตรอนนั้นเข้าไปอยู่ในระดับพลังงานที่ 4 เพราะการจัดเรียงอิเล็กตรอน อิเล็กตรอนชั้นนอกสุดซึ่งเรียกว่าเวเลนซ์อิเล็กตรอนต้องไม่เกิน 8





Comments
Post a Comment